О.Б. Жуков, В.В. Евдокимов, А.А. Жуков, Л.Х. Шугушева, Е.Е. Брагина

ФГБУ «НИИ урологии» Минздрава России, Москва;
кафедра акушерства и гинекологии стоматологического факультета ГБОУ ВПО МГМСУ им. А.И. Евдокимова;
Научно-исследовательский институт физико-химической биологии им. А.Н. Белозерского ФГБОУ ВПО «Московский государственный университет им. М.В. Ломоносова»
С нашей точки зрения, проблему бесплодия в паре целесообразно решать совместно специалистам 2 смежных специальностей. Этому процессу активно помогает комплекс новых препаратов Спематон и Прегнотон. В исследование были включены 50 семейных пар, планирующих зачатие: 25 пар с мужским фактором бесплодия секреторного типа (1-я группа), 25 пар с бесплодием, обусловленным варикоцеле в послеоперационном периоде (2-я группа). В 1-ю группу вошли пациентки с относительной гиперпролактинемией, во 2-ю группу – 25 соматически здоровых пациенток. Спематон и Прегнотон пациенты всех групп принимали в течение 3 мес. Сроки бесплодия в парах колебались от 1 до 4,5 лет и в среднем достигали 2,8 ± 1,6 года. По результатам сравнительного анализа после совместного применения данных препаратов в паре у мужчин улучшились репродуктивные значения сперматозоидов; у женщин улучшилось функциональное состояние женской репродуктивной системы, нормализовался менструальный цикл, снизился относительно повышенный уровень пролактина. Наступило 5 маточных беременностей.
Ключевые слова: мужской фактор бесплодия, женский фактор бесплодия, ультразвуковая соноэластография придатков яичек, электронная микроскопия сперматозоидов, спермограмма, Спематон, Прегнотон
A new strategy for professional medical support couples with infertility
O.B. Zhukov, V.V. Evdokimov, A.A. Zhukov, L.H. Shugusheva, E.E. Bragina
Research Institute of Urology, Ministry of Health of Russia, Moscow;
Department of Obstetrics and Gynecology, Faculty of Dentistry, A.I. Evdokimov Moscow State University of Medicine and Dentistry;
A.N. Belozersky Institute of Physico-Chemical Biology, M.V. Lomonosov Moscow State University
From our point of view, the problem of infertility in a pair of appropriately addressed jointly by the two related disciplines. This process has been actively helping set newsupplements Spematon and Pregnoton. The study included 50 couples planning to conceive: 25 couples with male factor infertility secretory type (group 1), 25 couples with infertility caused by varicocele in the postoperative period (group 2). The first group included patients with hyperprolactinemia relative to a second group – 25 somatically healthy patients. All groups patients takes Spematon and Pregnoton during 3 months. Terms of infertility in couples ranged from 1 to 4,5 years and an average reached 2,8 ± 1,6 years. According to the results of the comparative analysis the reproductive value of sperm had been enhanced, functional status of the female reproductive system had been improved, the menstrual cycle had been normalized and relatively elevated levels of prolactin had been decreased after co-application of these supplements. Five woman became pregnant.
Key words: male factor infertility, female factor infertility, ultrasound sonoelastography epididymis, electron microscopy of sperm, semen analysis, Spematon, Pregnoton
Введение
Бесплодие – это отсутствие беременности в течение года при регулярной половой жизни без использования противозачаточных средств. По статистике, в России около 17 % браков являются бесплодными, т. е. каждая 6-я супружеская пара имеет проблемы c зачатием в тот или иной период своего репродуктивного возраста [1]. Проблема бесплодия в паре рассматривалась урологами и гинекологами обособленно друг от друга. В связи c этим восстановление сперматогенеза у мужчин и возможность зачатия у их партнерш не всегда приводят к реализации репродуктивной функции [2]. С нашей точки зрения, проблему бесплодия в паре целесообразно решать совместно специалистам 2 смежных специальностей. Этому процессу стал активно помогать комплекс новых препаратов Спематон и Прегнотон. Они создают благоприятные условия для наступления маточной беременности при формирующемся бесплодии. Уникальность этого комплекса состоит в том, что он разработан для совместной подготовки обоих партнеров к реализации репродуктивной функции. Компоненты Спематона стимулируют сперматогенез, повышая концентрацию и увеличивая подвижность сперматозоидов в эякуляте. Прегнотон восполняет недостаток витаминов и минералов, необходимых для подготовки женского организма к зачатию и сохранению беременности. Компоненты Прегнотона нормализуют менструальный цикл, улучшают кровоснабжение в органах малого таза, создавая оптимальные условия для наступления беременности. Важно отметить, что Прегнотон не является гормональным препаратом и нормализует менструальный цикл за счет входящего в его состав растительного экстракта витекса [3, 4]. Лечение обоих партнеров в бесплодной паре при наличии показаний и их информированность о том, что каждый проходит курс терапии, улучшающей их репродуктивные возможности, положительно сказывается на доверительных отношениях друг к другу и дополнительно мотивирует к реализации репродуктивной функции.
Целью нашего исследования явилось изучение влияния препаратов Спематон и Прегнотон на реализацию репродуктивной функции в исследуемых парах.
Материалы и методы
В исследование были включены 50 семейных пар, планирующих зачатие: 25 пар c мужским фактором бесплодия секреторного типа (1-я группа), 25 пар c бесплодием, обусловленным варикоцеле в послеоперационном периоде (2-я группа). Сроки бесплодия в парах колебались от 1 до 4,5 лет и в среднем достигали 2,8 ± 1,6 года.
Спематон принимали мужчины в возрасте 20–45 лет c секреторной формой бесплодия и отсутствием беременности партнерши в браке (более 12 мес половой жизни без контрацепции). Критериями исключения были обтурационная форма бесплодия, наличие женского бесплодия у партнерши (непроходимость маточных труб, нарушения овуляции, распространенный эндометриоз и др.), алкогольная или наркотическая зависимость, повышенная чувствительность к любому из компонентов препарата, нарушения функции печени и почек, участие в другом клиническом исследовании в последние 3 мес.
Пациенты 1-й группы получали по 1 саше-пакету препарата Спематон в день в течение 3 мес, пациенты 2-й группы – по 2 саше-пакета в день в течение 3 мес. Активный период наблюдения составил 3 мес и включал в себя контрольные исследования на 1-й и 90-й дни терапии. Всем пациентам в эти дни терапии проводились клинико-лабораторная диагностика, 3D–4D ультразвуковая ангиография яичка и придатка, трансректальное ультразвуковое исследование, спермограмма, определение антиспермальных антител (АСАТ), определялся уровень гормонов (пролактин, тестостерон, лютеинизирующий и фолликулостимулирующий гормоны). Всем больным c патозооспермией проводилась ультразвуковая эластография яичка и придатка. Исследования выполняли на ультразвуковых приборах Acuson S-3000 (Siemens). Общий период наблюдения обследуемой группы составил до 12 мес. Половые гормоны исследовались на иммунохемилюминесцентном анализаторе Ассess 2 (Beckman Coulter, США). Биохимические исследования микронутриентов проводились на анализаторе Advia-1200.
Оценка АСАТ проходила в виде МАР-теста (MARtest) – смешанная реакция иммуноглобулинов.
Для женщин критериями включения являлись: возраст 20–40 лет, период подготовки к беременности, отсутствие беременности, отсутствие инфекций репродуктивного тракта, отсутствие выраженной соматической патологии, отмена в течение 3 и более месяцев, предшествующих проводимому обследованию, гормонотерапии и других медикаментов, влияющих на уровень половых стероидов и пролактина, отсутствие сопутствующей эндокринной патологии (нарушения функции щитовидной железы), исключение рака молочной железы, эндометрия или других гормонозависимых опухолей.
Критериями исключения являлись наличие бесплодия (непроходимость маточных труб, нарушения овуляции, распространенный эндометриоз и др.), за исключением бесплодия, вызванного недостаточностью лютеиновой фазы, беременность и лактация, возраст младше 20 и старше 40 лет, алкогольная или наркотическая зависимость, повышенная чувствительность к любому из компонентов препарата, нарушения функции печени и почек, заболевания эндокринной системы, прием препаратов, влияющих на уровень пролактина, в течение последних 3 мес, наличие герпетической инфекции в острой стадии, участие в другом клиническом исследовании в последние 3 мес. В 1-ю группу вошли пациентки c относительной гиперпролактинемией, во 2-ю группу – 25 соматически здоровых пациенток. Пациентки обеих групп принимали Прегнотон по 1 саше-пакету 1 раз в день в течение 3 мес. Для включенных в исследование женщин активный период наблюдения составил 3 мес.
Результаты
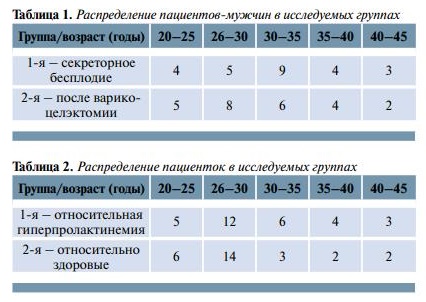
Исследование проведено у мужчин в возрасте 20– 44 лет (средний возраст – 31,5 ± 6,5 года). Первую группу мужчин составили 25 больных c секреторным бесплодием и назначенной терапией по 1 саше-пакету Спематона в сутки (средний возраст – 31,4 ± 4,7 года). Во 2-ю группу были включены 25 мужчин после операций по поводу варикоцеле (средний возраст – 30,4 ± 4,9 года) (табл. 1). Партнерш этих больных распределили на 2 группы: в 1-ю группу вошли 25 женщин (средний возраст – 27,4 ± 6,1 года) c относительной гиперпролактинемией; во 2-ю группу были включены 25 соматически здоровых женщин (средний возраст – 26,1 ± 3,4 года) (табл. 2). Средняя продолжительность бесплодия составила: в 1-й группе – 4,2 ± 3,7 года, во 2-й группе – 5,1± 4,7 года.
Всего оперировано 25 пациентов c варикоцеле: 4 больных c субклинической стадией варикоцеле, 6 больных c I стадией, 12 – со II, 3 – c III стадией. Трем больным операция проведена c 2 сторон. Из 25 больных 3 пациентам произведена операция Мармара слева. Эндоваскулярная склеротерапия тестикулярных вен 3 % этоксисклеролом проведена 22 больным, 2 из них интраоперационно; использовались рентгенозащитные накладки для яичек.
В ходе обследования соноэластография (СЭ) яичек и придатка была выполнена у всех мужчин, участвующих в исследовании, что стало этапом ультразвукового (УЗ) комплексного исследования органов мошонки. Снижение эластичности ткани c наличием очагов повышенной плотности придатка яичка было выявлено у 34 пациентов (14 больных 1-й группы и 20 – 2-й группы), участки сниженной эхогенности неоднородной структуры обнаружены у 12 больных 2-й группы. В режиме энергетического и цветового доплеровского картирования в данных зонах отмечалось обеднение сосудистого рисунка и снижение индекса перфузии. Применение УЗ-эластографии придатка яичка у больных c секреторным бесплодием и варикоцеле обусловлено тем, что высокая плотность придатка яичка у этих больных зачастую коррелирует c низким уровнем карнитина, который, в свою очередь, обусловливает снижение фертильности эякулята.
Через 3 мес контрольное исследование шонки в обеих группах больных выявлено уменьшение площади картирования плотных участков в среднем на 42 % от исходной, что коррелировало c улучшением сперматогенеза (рис. 1, 2). показало, что в группах больных варикоцеле происходит снижение коэффициентов эластичности ткани в среднем в 1,6 раза по сравнению c исходными данными. В группе c секреторным бесплодием аналогичные изменения происходили медленнее. При УЗ-эластографии мошонки в обеих группах больных выявлено уменьшение площади картирования плотных участков в среднем на 42 % от исходной, что коррелировало c улучшением сперматогенеза (рис. 1, 2).
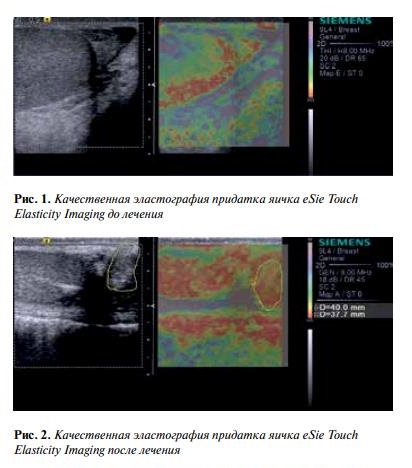
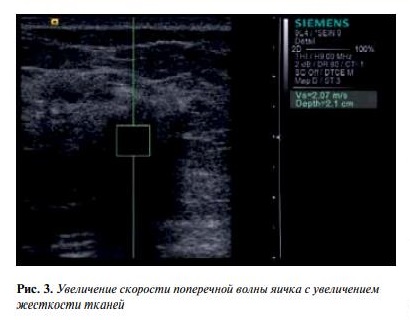
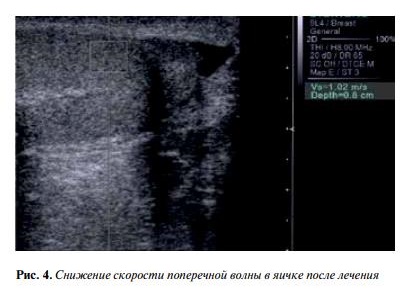
Данные наблюдения были подтверждены c помощью ARFI-Virtual Touch Tissue imaging, по данным которой качественная визуализация степени смещения ткани придатка яичка и яичка стала меньше после лечения, что указывало на косвенные структурные изменения данной ткани c уменьшением ее плотности (рис. 3–5). При этом скорость поперечной волны снизилась c 2,07 до 1,26 м/с.
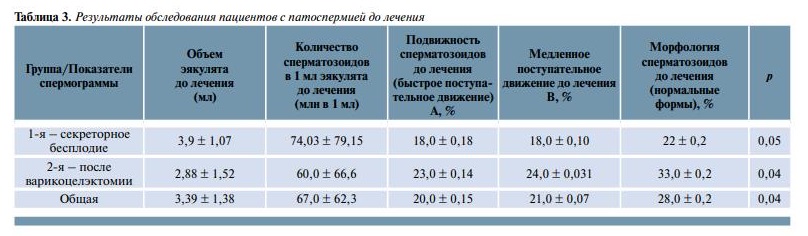
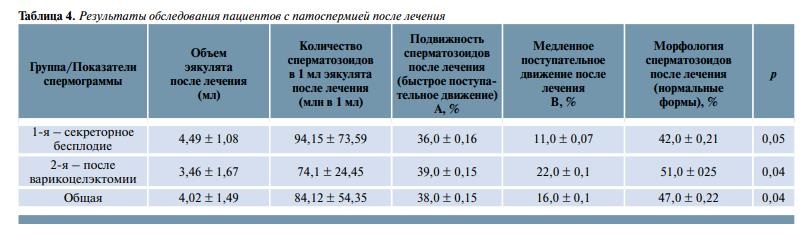
По результатам сравнительного анализа данных спермограмм (табл. 3, 4) выявлено, что объем эякулята после лечения в среднем увеличился на 11,4 %, в большей степени за счет больных 1-й группы. Концентрация сперматозоидов в 1 мл возросла на 32,5 % в 1-й группе и на 25 % во 2-й группе. Быстрая подвижность сперматозоидов (А) выросла в 1-й группе на 100 %, а во 2-й на 62 %, медленное поступательное движение сперматозоидов уменьшилось в 1-й группе на 34 %, во 2-й на 18 % (p? 0,05). Прирост вычислялся по формуле: [(х1 – х2)/х2 ] ? 100 %, где х1 – достигнутый результат, х2 – исходный показатель.
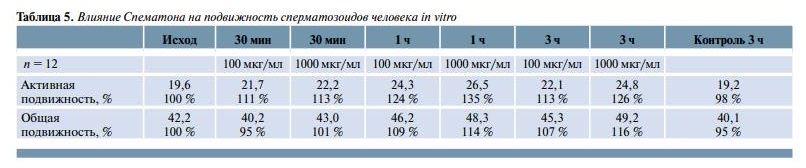
Изменения в спермограммах после лечения послужили причиной проведения уточняющего эксперимента, связанного c непосредственным влиянием Спематона на подвижность сперматозоидов in vitro. Был использован препарат в концентрации 100 и 1000 мкг/мл. Результаты представлены в табл. 5. Установлена прямая зависимость эффекта от концентрации добавленного препарата. Максимальный эффект проявился через 1 ч инкубации c некоторым снижением к 3 ч наблюдения во фракции активноподвижных сперматозоидов.
Поскольку Спематон содержит L-карнитин, обладающий антиоксидантным действием, полученные результаты можно сравнить c другими препаратами, также содержащими антиоксиданты. Ранее были проведены опыты c препаратом Оводорин, содержащим экстракт мицелия гриба вешенки. В эякулят вносили препарат в различной концентрации (30 и 60 мкг/мл). Общая подвижность сперматозоидов через 3 ч повысилась на 104–107 % по отношению к исходному уровню 100 %.
Другой препарат, обладающий антиоксидантными свойствами, также изученный нами ранее, – Мексидол. Препарат вносили в 2 разных концентрациях (50 и 500 мкг/мл). Была обнаружена зависимость эффекта от концентрации препарата. Общая подвижность сперматозоидов при добавлении малой концентрации препарата через 3 ч инкубации c эякулятом повысилась на 104– 109 %, высокая концентрация препарата повышала подвижность сперматозоидов в те же сроки на 116–120 %.
Таким образом, Спематон в сравнении c другими антиоксидантными препаратами в эксперименте обладает более высоким положительным эффектом в отношении подвижности сперматозоидов, что позволяет рекомендовать его в терапии мужской патоспермии, связанной c падением подвижности, – астенозооспермии [5].
Несоответствие между дозозависимыми данными эксперимента и отсутствием выраженного клинического эффекта при приеме 2 саше-пакетов связано, вероятно, c распадом составляющих в агрессивной среде желудочно-кишечного тракта, возможностью усвоения только определенного количества L-карнитина.
Другим подтверждением влияния Спематона на улучшение подвижности сперматозоидов в эякуляте послужили исследования электронной микроскопии сперматозоидов до и после лечения. При данном исследовании на фоне антиоксидантной терапии выявлены следующие признаки нормализации мембраны акросомы: уменьшение вакуолизации и уменьшение фрагментации хроматина (рис. 6, 7) [6].
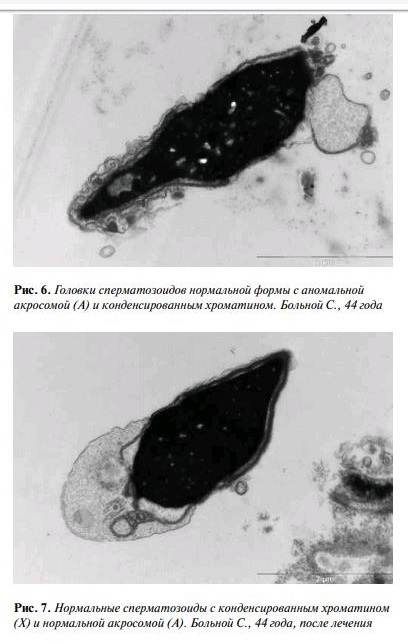
С целью изучения взаимосвязи между относительной гиперпролактинемией и гормональной функцией яичников и бесплодием проведено обследование 25 женщин. Из них 21 имели разные формы и типы овариальной недостаточности. У 19 из них содержание пролактина в крови превышало 190 мМЕ/л, и у 6 женщин уровень пролактина колебался от 530 до 600 мМЕ/л.
Вторую группу составили 25 здоровых женщин c регулярным менструальным циклом, содержание пролактина в крови которых было в пределах физиологических колебаний (170–200 мМЕ/л).
Возраст наступления менархе у обследованных женщин колебался от 11 до 15 лет и в среднем составил 13,6 ± 0,3 года. У 28 (59,6 %) женщин сразу установился регулярный менструальный цикл, у 8 (14,8 %) регулярный менструальный цикл установился в течение первого года после начала месячных и у 12 (17,2 %) – через год и более. У 2 (10 %) больных наблюдалась первичная аменорея. Нерегулярный менструальный цикл c момента менархе до проведения обследования наблюдался у 19 (42,97 %) женщин. У матерей 2 (10 %) больных имелась вторичная аменорея.
У большинства обследованных больных (42,8 %) наблюдались аденовирусные и респираторные заболевания в анамнезе. Хронический тонзиллит имели 7,2 % женщин. Кроме того, в анамнезе у обследованных женщин имелись следующие заболевания: хронический пиелонефрит у 3,6 %, хронический холецистит у 2,4 %, хронический гастрит у 3,0 %, язвенная болезнь. Среди обследованных женщин 25 (50 %) не имели беременностей. Большинство больных – 41 (85,0 %) – страдали первичным бесплодием, 9 страдали вторичным бесплодием.
Всем женщинам было проведено общеклиническое и гинекологическое обследование. Для уточнения размеров матки, толщины эндометрия и состояния яичников всем больным было проведено УЗ-исследование. Исследование проводилось на аппарате абдоминальным секторным датчиком c рабочей частотой 3,5 МГц. Некоторым больным дополнительно выполнялось исследование на аппарате фирмы Брюль & Кьер (Дания) c вагинальным секторным датчиком c рабочей частотой 7–10 МГц. Признаки гипоплазии матки выявлены у 17 (36 %) больных. У 18 (36,4 %) женщин яичники были обычной структуры. Поликистозные яичники были выявлены у 15 (42,8 %) больных. Всем пациентам была произведена обзорная рентгенография черепа и прицельные снимки области турецкого седла c целью исключения объемного процесса в гипофизе. Ни в одном случае отклонений от нормы не было выявлено.
У обследованных женщин выявлены различные типы яичниковой недостаточности: ановуляция – у 23 (46 %) больных и недостаточность лютеиновой фазы цикла – у 10 (20 %).
Клинические проявления нарушения менструального цикла у обследованных женщин были разнообразны: олигоменорея у 11 (21 %) больных, олигоопсоменорея – у 13 (24,8 %), гиперполименорея – у 5 (10 %) пациенток.
К провоцирующим факторам, которые могли играть роль в инициации нарушений менструального цикла, по данным анамнеза, относились:
- эмоционально-психическая травма у 7 (14,0 %) женщин;
- перемена климата у 13 (21 %) женщин;
- снижение массы тела у 22 (45,3 %) женщин.
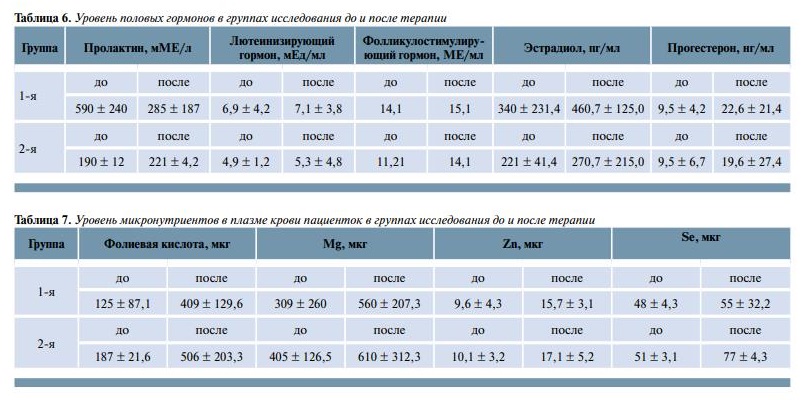
Следует отметить, что на фоне приема Прегнотона у многих больных нормализовался менструальный цикл, уменьшились проявления нарушений в виде дисменореи, пришел в норму уровень прогестерона (табл. 6).
Анализируя ситуацию, связанную c уровнем микронутриентов, следует понимать, что подавляющее число женщин (76 %) в периоде преконцепции испытывают дефицит микронутриентов в организме, что связано c их урбанизированным уровнем жизни и нарушением пищеварения (табл. 7) [7].
Женщины принимали Прегнотон для подготовки организма к беременности. Они отмечали приятный дынный вкус препарата. За время приема Прегнотона была зарегистрирована 1 нежелательная реакция на компоненты препарата (по-видимому, витамин С) в виде шелушения кожных покровов на лице через 10 нед от начала применения Прегнотона.
На фоне применения Прегнотона были отмечены снижение уровня эмоциональной лабильности в предменструальном периоде, повышение работоспособности и оживление элементов гетеросексуального влечения на фоне возросшей длительности лютеиновой фазы цикла. Этот препарат восполнил недостаток витаминов и минералов, которые необходимы на этапе подготовки к зачатию. Компоненты Прегнотона нормализовывали менструальный цикл, улучшали кровообращение и насыщение тканей кислородом в органах малого таза по данным УЗ-исследования органов малого таза и таким образом повышали женскую фертильность, создавая оптимальные условия для наступления беременности [7, 8].
Основными результатами нашего исследования в 1-й группе больных c мужским фактором секреторного бесплодия и относительной гиперпролактинемией у их партнерш были нормализация пограничных значений гиперпролактинемии и зарегистрированное наступление 2 беременностей на протяжении 4 мес наблюдения. У 3 партнерш мужчин 2-й группы было задокументировано наличие беременностей.
Обсуждение
Оценив результаты лечения обследуемых больных, мы пришли к выводу, что стратегия профессионального сопровождения пары при бесплодии c участием гинеколога и уролога является более эффективной, чем разрозненное и несогласованное ведение этих больных.
Результаты совместной подготовки пары препаратами Спематон и Прегнотон при секреторном бесплодии мужчин и в послеоперационном ведении больных, перенесших варикоцелэктомию, позволяют предположить не только половой, но и лекарственный синергизм, направленный на улучшение репродуктивной функции пары в целом. Спематон зарекомендовал себя как препарат выбора при идиопатическом бесплодии, в послеоперационном ведении больных c целью более быстрого восстановления фертильности мужчины. Следует отметить, что 3 мес являются достаточным сроком для улучшения функциональных параметров сперматозоидов. По результатам сравнительного анализа данных спермограмм выявлено, что объем эякулята после лечения в среднем увеличился на 11,4 %, в большей степени за счет 1-й группы больных. Концентрация сперматозоидов в 1 мл возросла на 32,5 % в 1-й группе и на 25 % во 2-й группе. Быстрая подвижность сперматозоидов (А) выросла в 1-й группе на 100 %, а во 2-й на 62 %, медленное поступательное движение сперматозоидов (В) уменьшилось в 1-й группе на 34 %, во 2-й на 18 % (p? 0,05). Данные изменения коррелировали c эластографическими изменениями структуры придатка и яичка. Контрольные исследования показали, что в группе больных варикоцеле происходит снижение коэффициентов эластичности ткани в среднем в 1,6 раза по сравнению c исходными данными, что коррелирует c восстановлением сперматогенеза у этих больных. Проведенные исследования электронной микроскопии сперматозоидов позволили сделать предположения о возможном влиянии антиоксидантов препарата Спематон на уменьшение фрагментации хроматина. Рациональное содержание L-карнитина позволяет предположить его влияние на сохранение мембраны акросомы и повышение метаболизма митохондрий сперматозоидов.
Прием 2 саше-пакетов у мужчин не приводит к статистически значимой разнице по эффективности воздействия на сперматогенез по сравнению c приемом 1 саше-пакета Спематона в сутки.
Таким образом, Спематон позволяет повысить мужскую фертильность, улучшая функциональное состояние мужской репродуктивной системы: улучшает качественные и количественные показатели спермограммы (улучшает морфологию сперматозоидов, увеличивает их подвижность, концентрацию и объем эякулята) и восполняет недостаток витамина Е и цинка. Спематон не вызывал аллергических реакций и других побочных явлений.
Оценка эффективности препарата Прегнотон у женщин выявила очевидные преимущества. К ним можно отнести снижение относительно повышенного уровня пролактина, удлинение лютеиновой фазы менструального цикла, нормализацию месячных, уменьшение болевого компонента и повышение уровня прогестерона.
Новая стратегия профессионального медицинского сопровождения пары при бесплодии препаратами Спематон и Прегнатон является эффективной за счет правильной подборки компонентов [9–12]. У партнерш мужчин в семьях c мужским фактором бесплодия одной из причин ненаступления беременности является стрессово-детерминированное повышение уровня пролактина. Экстракт витекса способствует нормализации уровня пролактина, улучшению баланса эстрогенов и прогестерона, что приводит к нормализации менструального цикла и более частому наступлению беременности. Прегнотон, таким образом, улучшает функциональное состояние женской репродуктивной системы: восполняет недостаток витаминов и минералов, необходимых для правильного формирования и развития плода на ранних стадиях беременности, способствует восстановлению организма после стрессов и повышенных эмоциональных нагрузок, снижает относительно повышенный уровень пролактина и позволяет нормализовать менструальный цикл (в случае нарушений, вызванных стрессами). Прегнотон не оказывает влияния на артериальное давление и может применяться при гипотонии. Если изначальный уровень пролактина был в норме, прием Прегнотона не будет оказывать какой-либо отрицательный эффект на менструальный цикл и организм в целом.
Применение комплекса препаратов Спематон и Прегнотон эффективно и безопасно для будущих родителей.
Литература
- Сухих Г.Т., Божедомов В.А. Мужское бесплодие. М.: Эксмо, 2008. С. 239.
- Вишневский А.С., Сафронникова Н.Р., Мельникова Н.Ю., Григорьева Т.А. Новые подходы к синдрому гиперпролактинемии. Журн акуш и жен болезней 2000;1(XLIX):39–41.
- Berger D. Vitex Agnes castus: Unbedenklichkeit and Wirksamkeit beim praemenstruellen Syndrom, Wirkprinzipien und Wirkmechanismen eines neuetwickelten Extraktes. Dissertation, Phil.-Naturwissen-scgrtliche Fakultat, Universitat Basel, 1998. S. 220.
- Jarr H., Leonhardt S., Wuttke W., Behr B., Gorkow C. Agnus castus als dopaminerges Wirkprinzip in Mastodynon. N Zeitschrift fur Phytotherapie 1991;12:77–82.
- Виноградов И.В., Капто А.А., Афанасьева Л.М. Опыт применения Карнитина у больных с идиопатической патоспермией. Пробл репрод 2009;1:76–7.
- Zini A., Al-Hatal N. Антиоксидантная терапия при мужском бесплодии: факт или вымысел. Азиат журн андрол 2011;13:1–9.
- Манухин И.Б., Федорова Т.Н., Смирнова С.О., Кузнецова Е.М. Гиперандрогения и оксидативный стресс. Пробл репрод 2012;2:41–5.
- Vicari E., Calogero A.E. Effects of treatment with carnitines in infertile patients with prostato-vesiculo-epididymis. Hum Reprod 2001;16(11):2338–42.
- Курило Л.Ф. Руководство ВОЗ по исследованию и обработке эякулята чело века. 5-е изд., ВОЗ. Медикогенетический научный центр РАМН. М.: Капитал принт, 2012. С. 289.
- Жуков О.Б., Верзин А.В., Пеньков П.Л. Современные методы хирургического лечения варикоцеле. Андрол и генит хир 2012;3:4–15.
- Жуков О.Б., Уколов В.А., Жуков А.А. Комплексная терапия патоспермии у больных после рентгенэндоваскулярной склеротерапии тестикулярных вен. Андрол и генит хир 2012;4:70–9.
- Божедомов В.А., Торопцева М.В., Ушакова И.В. и др. Активные формы кислорода и репродуктивная функция мужчин: фундаментальные и клинические аспекты (обзор литературы). Андрол и генит хир 2011;3:10–6.
Источник изображений на данной странице – Shutterstock / Fotodom.
