Современные представления о формировании наружного генитального эндометриоза
Роль индол-3-карбинола и транс-ресвератрола в модификации терапии наружного генитального эндометриоза.
Раздел «Специалистам» предназначен исключительно для медицинских и фармацевтических работников. Если вы не являетесь медицинским или фармацевтическим работником, посетите другие разделы сайта, например, «Статьи».

Роль индол-3-карбинола и транс-ресвератрола в модификации терапии наружного генитального эндометриоза.
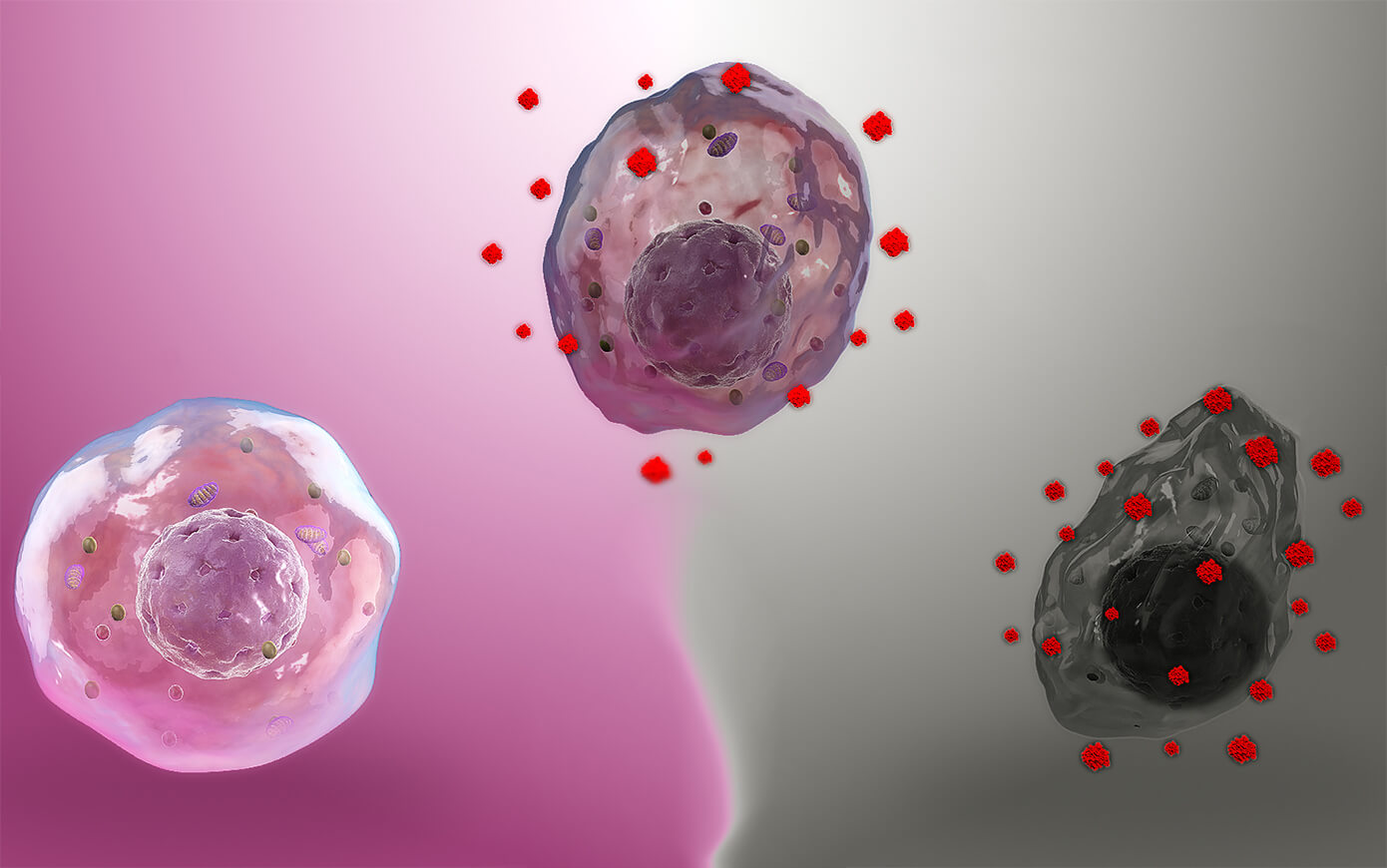
В обзоре представленны данные, которые свидетельствуют о необходимости включения в комплекс лечебных мероприятий у пациенток с эндометриозом антиоксидантных средств, способных подавить ряд важных проявлений оксидативного стресса.

Рассмотрены механизмы формирования боли при эндометриозе, а также возможности патогенетического влияния транс-ресвератрола и индол-3-карбинола на различные аспекты эндометриоз-ассоциированного болевого синдрома.
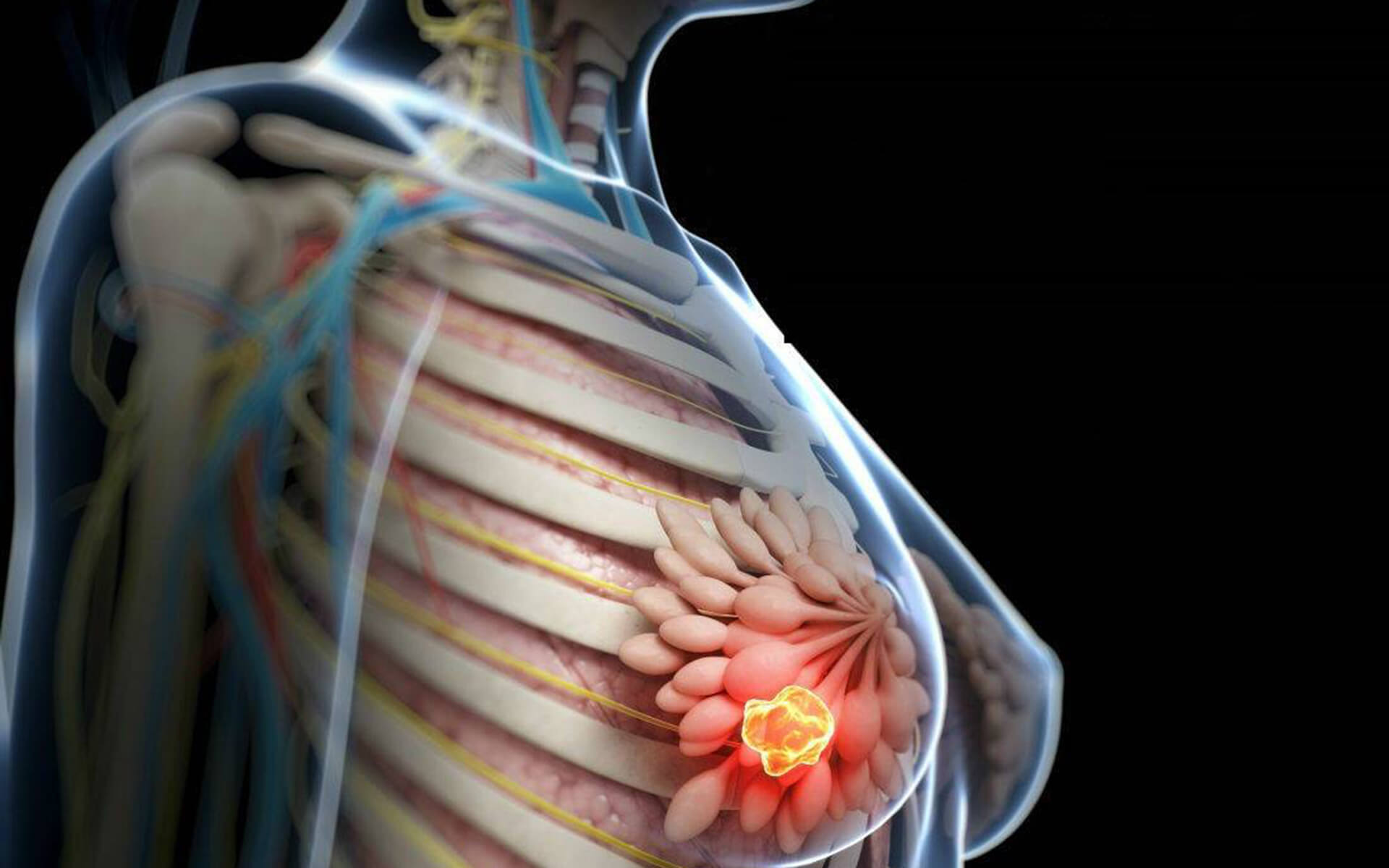
Рассматривается возможность комбинированного применения ресвератрола и индол‑3-карбинола для терапии циклической масталгии и ДДМЖ в целях улучшения качества жизни и профилактики злокачественных новообразований.
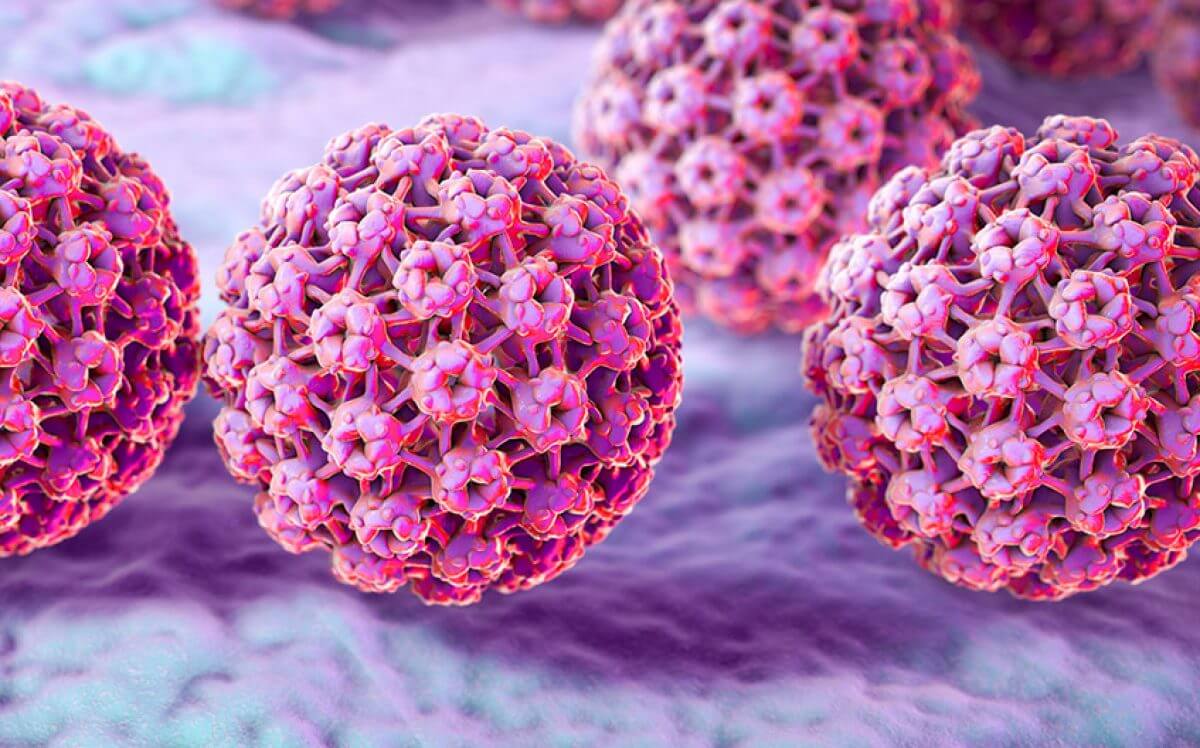
Описаны положительные терапевтические эффекты ресвератрола и индол-3-карбинола (И3К), способные значительно снизить вероятность развития и прогрессирования ВПЧ-ассоциированных заболеваний аногенитальной области.

В обзоре представлены современные данные о применении транс-ресвератрола и индол-3-карбинола при наружном генитальном эндометриозе и аденомиозе как в экспериментальных моделях, так и в клинической практике.

Рассматриваются стрессовые факторы, способные повлиять на менструальный цикл, и оцениваются возможности средств, повышающих резерв адаптации, в коррекции стресс-зависимых расстройств менструального цикла.
Описано медикаментозное купирование симптомов аденомиоза, включающее прием препаратов для нормализации работы антиоксидантной системы, к которым относится комплекс индол-3-карбинола и ресвератрола (Имастон).

Исследование ВМК «Прегномама» с точки зрения его эффективности для поддержания психофизиологического состояния при нормально текущей беременности и безопасности в течение всей беременности.
Представлены результаты исследования, целью которого была оценка состояния молочных желез у женщин пременопаузального возраста с гиперплазией эндометрия на фоне применения индол-3-карбинола (I3C).

Описывается сочетанное применение альфа-липоевой кислоты с мио-инозитолом и Д-хиро-инозитолом в качестве комплексной стратегии по преодолению инсулинорезистентности и ее последствий у женщин с синдромом поликистозных яичников.

Приведен анализ проблемы и отражен опыт использования витаминно-минерального комплекса с экстрактом витекса священного с целью прегравидарной подготовки у пациенток с функциональной гиперпролактинемией на фоне хронического стресса.